Страницы сайта
Текущий курс
Участники
Курс неорганической химии
Ученикам. Как работать в системе Мооdle
Введение в предмет химии.
Глава 1. Атомы химических элементов
Глава 2. Простые вещества.
Глава 3. Соединения химических элементов
Глава 4. Изменения происходящие с веществами
Глава 5. Растворение. Растворы.
Глава 6
Тема 2. Изменения в составе ядер атомов химических элементов. Изотопы
Тема. Изменения в составе ядер атомов химических элементов. Изотопы.
Цель
формирование знаний о строении атома, умений определять величину заряда ядра, число электронов, протонов и нейтронов;
Cистематизация знаний о химическом элементе и периодической системе химических элементов.
Проверка знаний. Обоснуйте каждое утверждение:
1) Атом имеет сложное строение.
2) Атом электронейтрален.
3) Масса атома сосредоточена в ядре.
4) Ядро атома имеет положительный заряд.
5) Атом состоит из двух основных частей: ________ и ________. Ядро состоит из ________ и ________.
6) Заряд ядра атома определяется числом ________ в его составе и не зависит от числа ________.
7) Число электронов в атоме равно числу ________.
8) Атом элемента с порядковым № 20 имеет ________ электронов, ________ протонов, ________ нейтронов.
Изотопы
Разновидности атомов химического элемента с одинаковым зарядом ядра, но разным массовым числом называют изотопы. (С греческого isos – равный, topos – место, т.е. равноместные или занимающие одну клетку в периодической системе.)
Что такое изотоп и как получаются ионы
 Нам уже ясно, что все атомы состоят из протонов, нейтронов и электронов. Теперь предстоит разобраться, как из частиц всего трех видов получается все многообразие химических элементов и веществ, простых и сложных. Когда из элементарных частиц (так химики называют протоны, нейтроны и электроны) мы начинаем "конструировать" атомы, то надо собрать частицы всех сортов, причем в таких количествах, чтобы получился нужный результат - атом заданного элемента. Пока только неясно, какие из частиц для атома самые важные - протоны, нейтроны или электроны. Если для нас главное - химические свойства вещества, то самыми важными окажутся электроны. Сколько у атома электронов и как они расположены, какие у них манеры - ленивы они или энергичны, гуляки или домоседы? Вот что расскажет нам о характере и поведении каждого атома и в химических соединениях, и в химических реакциях. Но атом, как мы условились, должен быть электронейтральным. Значит, сколько электронов - столько и протонов. И все атомы, у которых одинаковое число протонов, будут считаться атомами одного и того же химического элемента: химические свойства у них тоже будут одинаковы. Значит, каждый химический элемент состоит из атомов с одним и тем же зарядом ядра, или с одним и тем же атомным номером.
Нам уже ясно, что все атомы состоят из протонов, нейтронов и электронов. Теперь предстоит разобраться, как из частиц всего трех видов получается все многообразие химических элементов и веществ, простых и сложных. Когда из элементарных частиц (так химики называют протоны, нейтроны и электроны) мы начинаем "конструировать" атомы, то надо собрать частицы всех сортов, причем в таких количествах, чтобы получился нужный результат - атом заданного элемента. Пока только неясно, какие из частиц для атома самые важные - протоны, нейтроны или электроны. Если для нас главное - химические свойства вещества, то самыми важными окажутся электроны. Сколько у атома электронов и как они расположены, какие у них манеры - ленивы они или энергичны, гуляки или домоседы? Вот что расскажет нам о характере и поведении каждого атома и в химических соединениях, и в химических реакциях. Но атом, как мы условились, должен быть электронейтральным. Значит, сколько электронов - столько и протонов. И все атомы, у которых одинаковое число протонов, будут считаться атомами одного и того же химического элемента: химические свойства у них тоже будут одинаковы. Значит, каждый химический элемент состоит из атомов с одним и тем же зарядом ядра, или с одним и тем же атомным номером.
А зачем же тогда нужны эти странные частицы нейтроны?
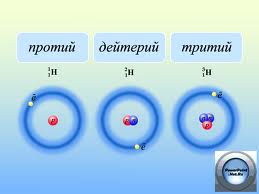
Оказывается, нейтроны, утяжеляя ядро атома, придают ему больше прочности. При этом в ядре атомов одного и того же элемента может содержаться разное число нейтронов. Например, в обычном атоме водорода 1 протон и 1 электрон. Такой атом водорода иначе называют "протий" и обозначают символом H. "Тяжелый водород" - дейтерий - содержит в ядре уже две крупные частицы: 1 протон и 1 нейтрон. Дейтерий имеет свой символ: D. Электрон у дейтерия один, как у обычного "легкого" водорода, поэтому по химическим свойствам дейтерий и протий одинаковы. Есть еще тритий - сверхтяжелый водород, в ядре атома которого, кроме протона, присутствуют 2 нейтрона. Электрон у трития тоже один. Тритий имеет свой особый химический символ: T.
Рис. Изотопы
"Легкий" водород (протий), дейтерий и тритий называются изотопами (от греческих слов "изос" - одинаковый и "топос" - место) элемента водорода. Они находятся в одной и той же клетке Периодической системы элементов, одинаковы по химическим свойствам, а отличаются только массой атома. Изотопы обозначают так:
Здесь мы видим слева от символа каждого изотопа две цифры - его числовые характеристики. Это цифры очень важные. Слева внизу указан порядковый номер данного элемента в Периодической системе, он же - заряд ядра, он же - число протонов. Наконец, он же дает нам общее число электронов в том атоме, о котором идет речь. Слева вверху стоит масса атома данного изотопа, выраженная в углеродных единицах.
Выводы урока
Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
Домашнее задание
Решение задачи: Что произойдет с атомами одного и того же вида, если в их ядра мысленно добавить по 1 протону? Теперь в ядро дейтерия добавьте один протон. Сравните атом дейтерия и полученную частицу. Какой заряд она имеет? Почему?
Интересно знать что ...